Данный документ содержит комплекс практических задач для студентов химико-технологических специальностей. Включает разделы: построение эмпирических моделей и регрессионный анализ, расчеты уравнений состояния реальных газов, моделирование фазовых равновесий многокомпонентных смесей, расчет химического равновесия в реакторах синтеза и составление материальных балансов сложных технологических схем. Задачи охватывают широкий спектр процессов от синтеза аммиака до разделения углеводородов.
- Тема 1: Эмпирические модели и регрессия
- Задача 2. Регрессионный анализ бензиновой фракции
- Задача 3. Уравнение Аррениуса
- Задача 4. Вязкость жидкостей
- Тема 2: Уравнения состояния и расчет однофазных потоков
- Тема 3: Расчет фазовых равновесий
- Задача 2. Расчет сепарационного блока
- Тема 4: Расчет химического равновесия
- Тема 5: Расчет материальных балансов
Тема 1: Эмпирические модели и регрессия
Задача 1. Поверхностное натяжение органических жидкостей можно оценить по эмпирическому выражению: σ = A · (1 - T/Tк)ⁿ. В таблице приведены измеренные значения поверхностного натяжения указанных жидкостей при соответствующей температуре. Определите параметры A и n эмпирической модели. С помощью эмпирической модели определите поверхностное натяжение при T = 385 К. Задача выполняется по вариантам.
| № вар. | Вещество | Тк (К) | 300 | 320 | 340 | 360 | 380 | 400 | 420 | 440 | 460 | 480 | 500 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 и 2 | этанол | 516.25 | 23.14 | 20.56 | 18.02 | 15.56 | 13.16 | 10.84 | 8.61 | 6.47 | 4.46 | 2.61 | 0.98 |
| 3 и 4 | 1-пропанол | 536.71 | 24.65 | 22.13 | 19.66 | 17.24 | 14.89 | 12.6 | 10.39 | 8.25 | 6.22 | 4.3 | 2.53 |
| 5 и 6 | метанол | 512.58 | 22.86 | 20.26 | 17.72 | 15.24 | 12.84 | 10.51 | 8.28 | 6.15 | 4.15 | 2.31 | 0.72 |
| 7 и 8 | циклогексан | 553.54 | 25.81 | 23.35 | 20.93 | 18.56 | 16.24 | 13.98 | 11.79 | 9.67 | 7.63 | 5.69 | 3.86 |
| 9 и 10 | бензол | 562.16 | 26.49 | 23.95 | 21.55 | 19.21 | 16.91 | 14.67 | 12.49 | 10.38 | 8.34 | 6.39 | 4.54 |
Задача 2. Регрессионный анализ бензиновой фракции
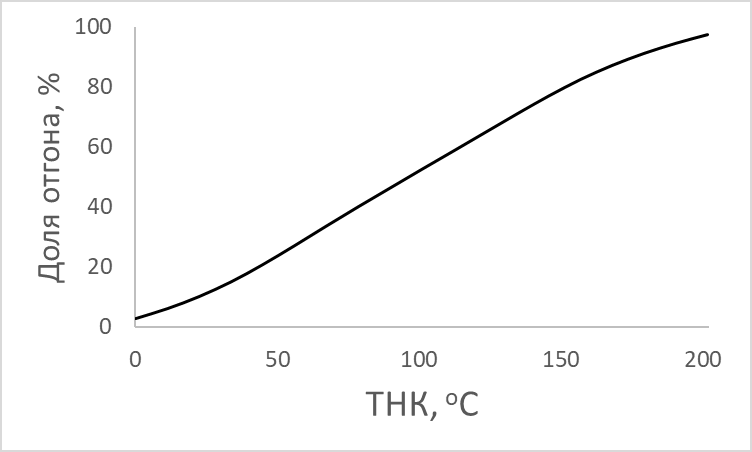
В таблице приведены данные разгонки широкой бензиновой фракции. Постройте серию эмпирических моделей в виде алгебраических степенных полиномов от 1-ой до 5-ой степени. Для каждого случая постройте график зависимости экспериментальных и модельных значений доли отгона от температуры начала кипения (ТНК). Оцените адекватность каждой модели, а также сравните модели между собой, рассчитав коэффициент детерминации и остаточную сумму.
| ТНК, оC | Доля отгона, % |
|---|---|
| 0.2 | 2.84 |
| 11.4 | 6.19 |
| 22.6 | 10.22 |
| 33.8 | 15.09 |
| 44.9 | 20.82 |
| 56.1 | 27.15 |
| 67.3 | 33.68 |
| 78.5 | 40.1 |
| 89.7 | 46.36 |
| 100.8 | 52.53 |
| 112 | 58.69 |
| 123.2 | 64.89 |
| 134.4 | 71.09 |
| 145.6 | 77.07 |
| 156.7 | 82.53 |
| 167.9 | 87.25 |
| 179.1 | 91.25 |
| 190.3 | 94.63 |
| 201.5 | 97.51 |
Задача 3. Уравнение Аррениуса
Зависимость константы скорости реакции от температуры для ряда веществ приведена в таблице. Рассмотрите возможность описания этой зависимости уравнением Аррениуса: k = A · e^(-Ea/(R·T)), где k – константа скорости, с⁻¹; A – предэкспоненциальный фактор, с⁻¹; Ea – энергия активации, Дж/моль; R – универсальная газовая постоянная Дж/(моль·К); T – температура, К. По приведенным данным определите константы уравнения Аррениуса – энергию активации и предэкспоненциальный фактор. Задачу необходимо решить с помощью Python.
| № вар. | 100 | 150 | 200 | 250 | 300 | 350 | 400 | 450 | 500 |
|---|---|---|---|---|---|---|---|---|---|
| 1 и 2 | 0.05 | 0.25 | 0.60 | 0.98 | 1.35 | 1.99 | 2.87 | 4.56 | 8.43 |
| 3 и 4 | 0.05 | 0.10 | 0.20 | 0.40 | 0.68 | 1.00 | 1.54 | 2.35 | 4.63 |
| 5 и 6 | 0.01 | 0.02 | 0.03 | 0.05 | 0.08 | 0.13 | 0.31 | 0.58 | 1.45 |
| 7 и 8 | 0.01 | 0.10 | 0.25 | 0.78 | 1.68 | 2.98 | 4.66 | 8.94 | 25.13 |
| 9 и 10 | 0.10 | 0.56 | 1.76 | 3.54 | 9.53 | 15.98 | 25.04 | 60.74 | 143.60 |
Задача 4. Вязкость жидкостей
В таблице приведены зависимости вязкости жидкости от температуры для ряда веществ. Постройте по приведенным данным эмпирическую модель с помощью Python. Оцените адекватность модели, рассчитав коэффициент детерминации, остаточную сумму. Постройте график зависимости экспериментальных и модельных значений динамической вязкости от температуры. Постройте и проанализируйте график остатков. С помощью построенной эмпирической модели определите динамическую вязкость при t = 57 0C.
| № вар. | Вещ-во | 250 | 260 | 270 | 280 | 290 | 300 | 310 | 320 | 330 | 350 | 370 | 390 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 и 2 | Ацетон | 0.500 | 0.442 | 0.395 | 0.356 | 0.322 | 0.293 | 0.268 | 0.246 | 0.230 | 0.200 | 0.170 | 0.150 |
| 3 и 4 | Бензол | — | — | 0.910 | 0.760 | 0.650 | 0.560 | 0.492 | 0.436 | 0.390 | 0.316 | 0.261 | 0.219 |
| 5 и 6 | Вода | — | — | 1.790 | 1.310 | 1.000 | 0.801 | 0.656 | 0.549 | 0.469 | 0.357 | 0.284 | 0.232 |
| 7 и 8 | Гексан | 0.497 | 0.426 | 0.397 | 0.355 | 0.320 | 0.290 | 0.264 | 0.241 | 0.221 | 0.190 | 0.158 | 0.132 |
| 9 и 10 | Глицерин | — | — | 12.00 | 8.500 | 6.050 | 4.250 | 3.500 | 2.600 | 2.000 | 1.200 | 0.730 | 0.450 |
Тема 2: Уравнения состояния и расчет однофазных потоков
Задача 1. Определите молярный объем аммиака при давлении 56 атм и температуре 450 К, используя уравнения: идеального газа, Редлиха-Квонга, Соаве-Редлиха-Квонга.
Задача 2. Имеется смесь, состоящая из 25% вещества 1, а оставшиеся вещество 2 и вещество 3 находятся в мольном соотношении 1:3. Рассчитайте мольный объем смеси, используя уравнения: идеального газа, Редлиха-Квонга, Соаве-Редлиха-Квонга. Сравните результаты. Объясните различия. Является ли газ идеальным?
| № вар. | Вещество 1 | Вещество 2 | Вещество 3 | Условия |
|---|---|---|---|---|
| 1 и 3 | аммиак | азот | водород | P = 270 атм, T = 550 К |
| 2 и 4 | диоксид углерода | монооксид углерода | водород | P = 175 атм, T = 500 К |
| 5 и 7 | пропилен | водород | пропан | P = 215 атм, T = 510 К |
| 6 и 8 | диоксид углерода | кислород | азот | P = 200 атм, T = 450 К |
| 9 и 10 | монооксид углерода | водород | метанол | P = 195 атм, T = 560 К |
Тема 3: Расчет фазовых равновесий
Задача 1. Рассчитайте температуры начала и конца кипения (в градусах Цельсия) следующей смеси при абсолютном давлении 14 атм: этилен (20%), этан (20%), пропан (40%), н-бутан (20%). Смесь можно считать идеальной.
Справочные данные для уравнения lnK = -A/T² + B - C·lnP + D/P + E/P² (P в psia, T в oR):
| Компонент | A | B | C | D | E |
|---|---|---|---|---|---|
| этилен | 600076.9 | 7.90595 | 0.84677 | 0 | 42.94594 |
| этан | 687248.2 | 7.90694 | 0.866 | 0 | 49.02654 |
| пропан | 970688.6 | 7.15059 | 0.76984 | 0 | 0 |
| н-бутан | 1280557 | 7.94986 | 0.96455 | 06.90224 | 0 |
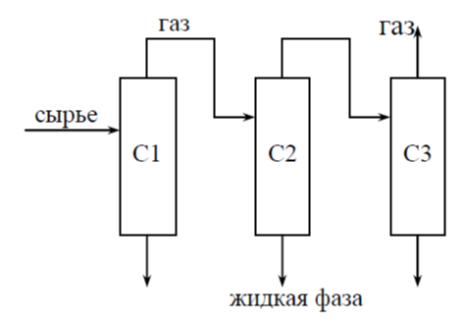
Задача 2. Расчет сепарационного блока
Провести расчет сепарационного блока
процесса разделения многокомпонентной углеводородной смеси (рассчитать состав и количество газовых и жидких потоков на выходе из каждого сепаратора) и исследовать влияние технологических параметров на процесс сепарации.
Базовые термобарические условия в сепараторах: P1 = 13.8 МПа, Т1 = 21.8 оС (С1); P2 = 9.7 МПа, Т2 = -8.6 оС (С2); P3 = 5.4 МПа, Т3 = -34.8 оС (С3).
| Компонент | Мольная доля | Молярная масса | Плотность газ | Плотность жидк. | Т. кип. | Т. крит. | P. крит. |
|---|---|---|---|---|---|---|---|
| CO2 | 0.004344 | 44 | 1.9650 | 859 | -78.2 | 304.2 | 72.83 |
| N2 | 0.021383 | 28 | 1.2510 | 570 | -195.8 | 126.2 | 33.5 |
| CH4 | 0.68525 | 16 | 0.7162 | 300 | -161.58 | 190.6 | 45.4 |
| C2H6 | 0.034238 | 30 | 1.3420 | 460 | -88.7 | 305.4 | 48.2 |
| C3H8 | 0.212213 | 44 | 1.969 | 501 | -42.06 | 369.8 | 41.9 |
| i-C4 | 0.006129 | 58 | 2.5948 | 557 | -11.73 | 408.1 | 36.0 |
| C4 | 0.004425 | 58 | 2.5948 | 580 | -0.5 | 425.9 | 37.5 |
| C5 | 0.006702 | 72 | 3.22 | 616 | 36.1 | 469.6 | 33.3 |
| Остаток | 0.021738 | 108 | 3.88 | 721 | 100.7 | 537.3 | 28.0 |
| H2O | 0.002891 | 18 | 0.804 | 1000 | 100 | 647.3 | 217.6 |
| CH3OH | 0.000686 | 32 | 2.678 | 791 | 64.65 | 512.6 | 79.9 |
Тема 4: Расчет химического равновесия
Задача 1. Найдите мольный расход каждого из веществ на выходе из реактора синтеза аммиака, если в реактор поступает смесь состава 1.1 : 3 : 0.2 = азот : водород : аммиак. Условия: Kp = 0.05, T = 589 K, P = 220 атм. Реакция: 1/2 N2 + 3/2 H2 ⇄ NH3.
Задача 2. Этилен получают нагреванием этана до высоких температур. В реактор поступает 100% этан. C2H6 ⇄ C2H4 + H2.
а) Определите равновесные концентрации этана, этилена и водорода при температуре процесса 1100 К и давлении в реакторе 1 атм. Константу равновесия определите по справочным данным.
б) Добавьте еще одну реакцию в процесс и повысьте температуру в реакторе до 1367 К. C2H4 ⇄ C2H2 + H2. Определите равновесный состав смеси, если константы равновесия Kp для указанных выше реакций при Т = 1367 К равны 37.6 и 0.769, соответственно.
Тема 5: Расчет материальных балансов
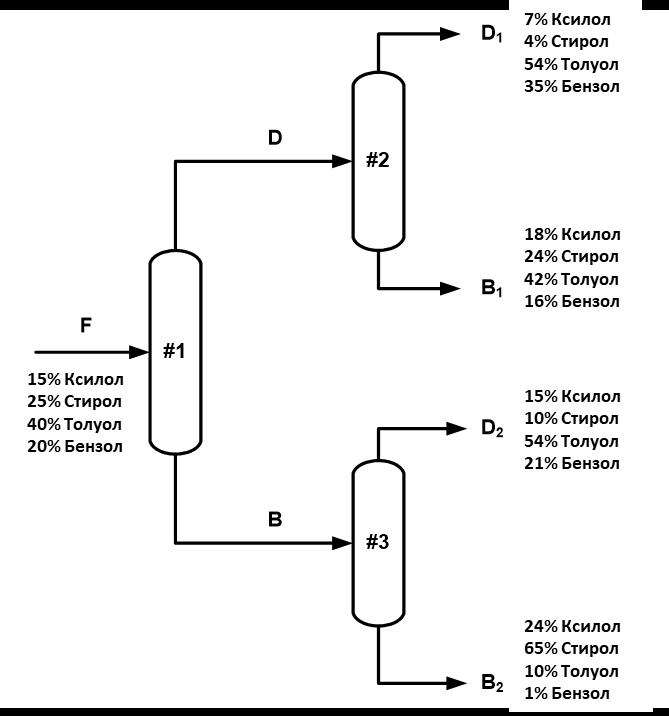
Задача 1. Найдите состав и мольный расход всех потоков на схеме разделения смеси ксилол, стирол, толуол, бензол
. На разделение поступает 1000 моль/ч сырья (поток F).
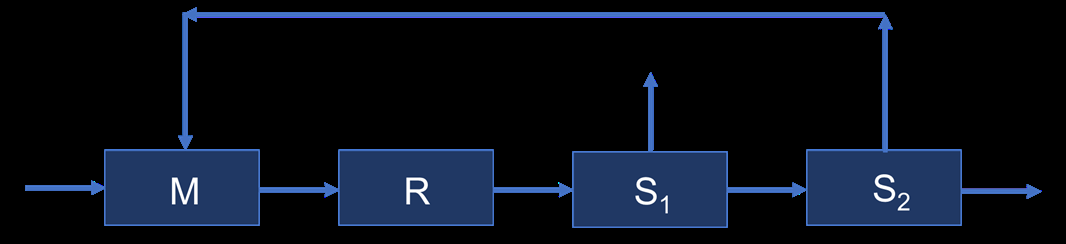
Задача 2. Процесс производства бензола из толуола показан на схеме
(процесс Toray, UOP). В процессе толуол (расходом 100 моль/ч) за счет реакции диспропорционирования (трансалкилирования) превращается в бензол и ксилол: 2C7H8 ⇄ C6H6 + C8H10. Конверсия за один проход в реакторе равна 58%.
Поток на выходе из реактора содержит все компоненты. Бензол отделяется, а толуол отправляется на рецикл. В первом разделителе поток бензола содержит 99.5% бензола поступившего в него, 0.1% толуола и не содержит ксилола. Во втором разделителе поток толуола, отправляющийся на рецикл, содержит весь бензол, 99.5% толуола и 0.1% ксилола, поступивших в разделитель. Рассчитайте материальный баланс процесса. Чему равна конверсия толуола в ксилол в этом процессе?